我们对质量、法规和合规的态度
它对我们和你的意义
在STEMCELL Technologies,我们投资于质量,以实现我们通过促进研究来推进科学知识的目标。为了确保我们始终符合最高的质量标准,我们运行符合相关和现行法规要求的质量管理体系(QMS),并不断努力改进我们的质量管理体系、产品和服务。
深入了解我们对质量的方法和承诺,以及我们如何支持您的监管和合规需求。
为什么质量很重要?
质量影响一切:产品性能和用户满意度,遵守法规要求和适用标准,以及我们作为一家公司的运作方式。确定您(使用我们产品的科学家)和相关监管机构可能存在的不同质量需求,对于设计满足这些要求的解决方案并确保您工作的可重复性、完整性和影响非常重要。
在STEMCELL,质量驱动着我们所做的一切。作为我们公司的核心价值观之一,这是我们文化中根深蒂固的一部分。
我们的质量方针基于以下原则:
- 质量意味着理解并超越您对我们产品和服务的期望
- 质量是可衡量和透明的
- 质量需要持续改进
- 质量被整合到整种产品管理生命周期中
- 质量从最高管理层开始
我们的品质方针
我们致力于:
- 卓越的产品质量和持续改进的客户服务驱动,客户满意,创新的科研。
- 遵守适用的法规要求,保持有效的质量管理体系。

我们的品质管理体系
质量管理体系(QMS)是实现质量方针和目标的过程、程序和职责的正式体系。它有助于协调和指导活动,以满足客户和法规要求,推动持续改进,并有助于努力提高客户满意度。
STEMCELL的质量管理体系已通过ISO 13485:2016医疗器械和ISO 9001:2015认证。这些国际标准是由独立的、非政府的国际标准化组织(ISO)制定的,规定了运行医疗器械设计和制造及相关服务的质量管理体系的要求。认证通过评估整种产品生命周期的输入和输出,从设计和生产到评估客户满意度和通知必要的改进,来验证这些标准是否得到满足。
有关这些ISO认证的更多信息和下载证书,请参阅我们的监管支持页面.
我们的质量管理体系通过了ISO 13485和ISO 9001认证,涵盖了以下关键领域:
- 培训员工有效地支持所有客户的科学和服务需求。
- 鉴定、校准和维护培养用于设计、制造和测试产品的设备。
- 保持严格的供应商资格,选择和管理过程。
- 要求组件和产品的全面可追溯性。
- 执行纠正和预防措施(CAPA)计划。
- 对所有关键流程进行定期内部审核。
我们的质量方针对您有何影响?
简而言之,我们将与您合作,确保满足您的特定要求,无论是性能还是监管要求。作为一个科学家帮助科学家的团队,我们的目的是帮助研究人员和组织最大限度地发挥他们的创新潜力。
我们致力于以卓越的产品性能和安全性以及个性化的客户服务超越您的期望。在我们持续改进、科学创新和法规遵从的过程导向方法中,您的满意也是优先考虑的。
您可以从我们这里期待什么:
- 作为制造高质量试剂和尖端研究工具的全球领导者,拥有超过25年的经验,包括对全球监管格局的了解以及它如何影响您的工作流程。
- 产品和服务对其预期用途是安全有效的,并且可靠地满足您的规格和要求。
- 按照相关法律、法规、标准和我们的质量管理体系设计、制造、销售和分销的产品和服务。
- 根据您的需求量身定制个性化的科学支持,从我们现成的解决方案问题到要求更高的合规性产品制造或定制产品。
- 帮助您满足法规遵从性需求的资源。
- 评估和减轻与使用我们的产品相关的可预见风险。
- 所有影响质量的活动的定义、计划和文档化。
质量和法规遵从性
在讨论产品质量时,重要的是要考虑产品性能和法规遵从性之间的差异。虽然经常混淆,但它们并不等同。例如,一个常见的误解是,遵循良好生产规范(GMP)是绝对必要的,以满足法规要求,并保证你的研究或制造工作流程中的产品性能。
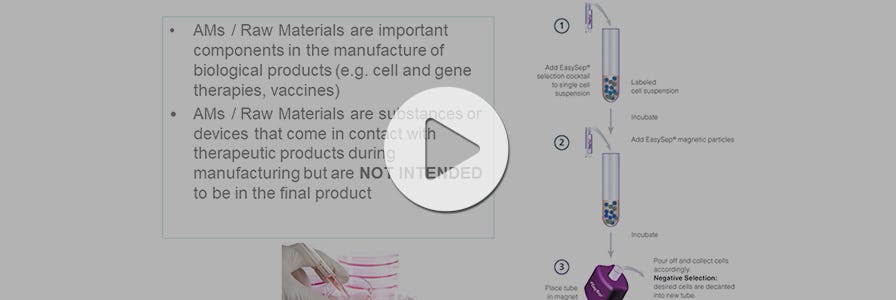
无论产品的合规性声明如何,重要的是与您的供应商和监管机构密切合作,以确保您选择的材料能够从性能和合规性两方面满足您的需求。这在选择和鉴定辅助材料(AMs;也称为原材料)用于制造细胞治疗产品,目前仍缺乏明确的法规。
随着研究人员越来越多地进入细胞疗法的转化领域,STEMCELL致力于通过支持他们继续使用我们的产品来缓解过渡。为了支持该领域不断变化的需求,我们还致力于扩大我们在不断增长的GMP计划中生产的产品目录。
通过遵循美国药典(USP)第1043章中概述的资格框架,STEMCELL可以支持我们的产品作为AMs使用,即使没有GMP。1我们的细胞治疗服务团队可以与您一起定义您的特定质量要求,并设计最适合您需求的解决方案。
如需了解有关细胞治疗制造合格AMs的常见问题的答案,并了解我们如何与您合作,请浏览我们的监管支持页面。你也可以联系我们或您的当地代表讨论您的具体法规或产品要求。
我们如何将质量最大化,风险最小化
在当今不断变化的经济和监管环境中,STEMCELL努力降低我们的业务和您的风险。我们通过风险管理的视角来优先考虑我们的项目、产品和过程。
我们的目标和对您的承诺是确保我们产品的不间断供应。通过投资风险管理计划,我们正在提高我们防止供应中断和快速应对意外风险的能力。
我们风险管理计划的关键要素包括:
- 有效的风险沟通计划,在内部业务单位和管理层之间建立风险意识。这使我们能够利用统一的、以优先级为基础的战略走在前面并减轻风险。
- 供应商管理计划,以确保我们的供应商符合STEMCELL的质量标准和业务要求。
- 一个强大的新产品引进流程,旨在确保整种产品生命周期的供应连续性。
- 符合iso14971医疗器械标准的关键产品风险管理文件。
- 一个自动库存管理系统,主动保持健康的库存水平和产品的可用性,为我们的客户。
- 面向客户和供应商的关系管理程序,以确保开放的沟通渠道和快速降低风险。
最小化风险包括持续改进。展望未来,我们将在现有风险管理框架的基础上,通过扩大对供应商社会和环境实践、地缘政治风险和绩效的考虑,来监控和降低风险。
产品生命周期管理
通过采用和维护培养一个强大的和负责任的过程,将产品从开发和制造转移到发布后的客户支持,我们始终如一地可靠地交付最高质量的产品。我们的重点是标准化,我们的客户已经开始期望我们的产品达到最高标准,具有极低的瓶对瓶或批次对批次的性能差异。
我们的产品管理生命周期包括以下正式阶段:
- 定义设计和测试需求
- 原型或试验批量制造
- 密集的质量控制测试
- 扩大
- 生产
- 稳定性测试
- 发布后的客户反馈
相关资源
探索这些额外的页面,以了解更多关于合格的辅助材料,我们的细胞治疗计划的服务,以及产品特定的质量信息。
参考文献
- 总论<1043>细胞、基因和组织工程产品的辅助材料。(2017)见:美国药典。